In den letzten Jahren wurden revolutionäre Fortschritte in der Behandlung von Adipositas und Typ-2-Diabetes erzielt. Nach GLP-1-Rezeptoragonisten (z. B. Semaglutid) und dualen Agonisten (z. B. Tirzepatid)Retatrutid(LY3437943), einDreifachagonist(GLP-1-, GIP- und Glucagonrezeptoren) hat eine beispiellose Wirksamkeit gezeigt. Mit bemerkenswerten Ergebnissen bei der Gewichtsreduktion und der Verbesserung des Stoffwechsels gilt es als potenzieller Therapiedurchbruch bei Stoffwechselerkrankungen.
Wirkungsmechanismus
-
GLP-1-Rezeptoraktivierung: Fördert die Insulinausschüttung, unterdrückt den Appetit, verzögert die Magenentleerung.
-
GIP-Rezeptoraktivierung: Verstärkt die blutzuckersenkende Wirkung von GLP-1 und verbessert die Insulinsensitivität.
-
Glucagon-Rezeptoraktivierung: Fördert den Energieverbrauch und den Fettstoffwechsel.
Durch die Synergie dieser drei Rezeptoren übertrifft Retatrutide bestehende Medikamente sowohl beim Gewichtsverlust als auch bei der Blutzuckerkontrolle.
Daten aus klinischen Studien (Phase II)
In einemPhase-II-Studie mit 338 übergewichtigen/adipösen PatientenRetatrutid zeigte äußerst vielversprechende Ergebnisse.
Tabelle: Vergleich von Retatrutid vs. Placebo
| Dosis (mg/Woche) | Durchschnittliche Gewichtsreduktion (%) | HbA1c-Reduktion (%) | Häufige unerwünschte Ereignisse |
|---|---|---|---|
| 1 mg | -7,2 % | -0,9 % | Übelkeit, leichtes Erbrechen |
| 4 mg | -12,9 % | -1,5 % | Übelkeit, Appetitverlust |
| 8 mg | -17,3 % | -2,0 % | Magen-Darm-Beschwerden, leichter Durchfall |
| 12 mg | -24,2 % | -2,2 % | Übelkeit, Appetitlosigkeit, Verstopfung |
| Placebo | -2,1 % | -0,2 % | Keine signifikante Änderung |
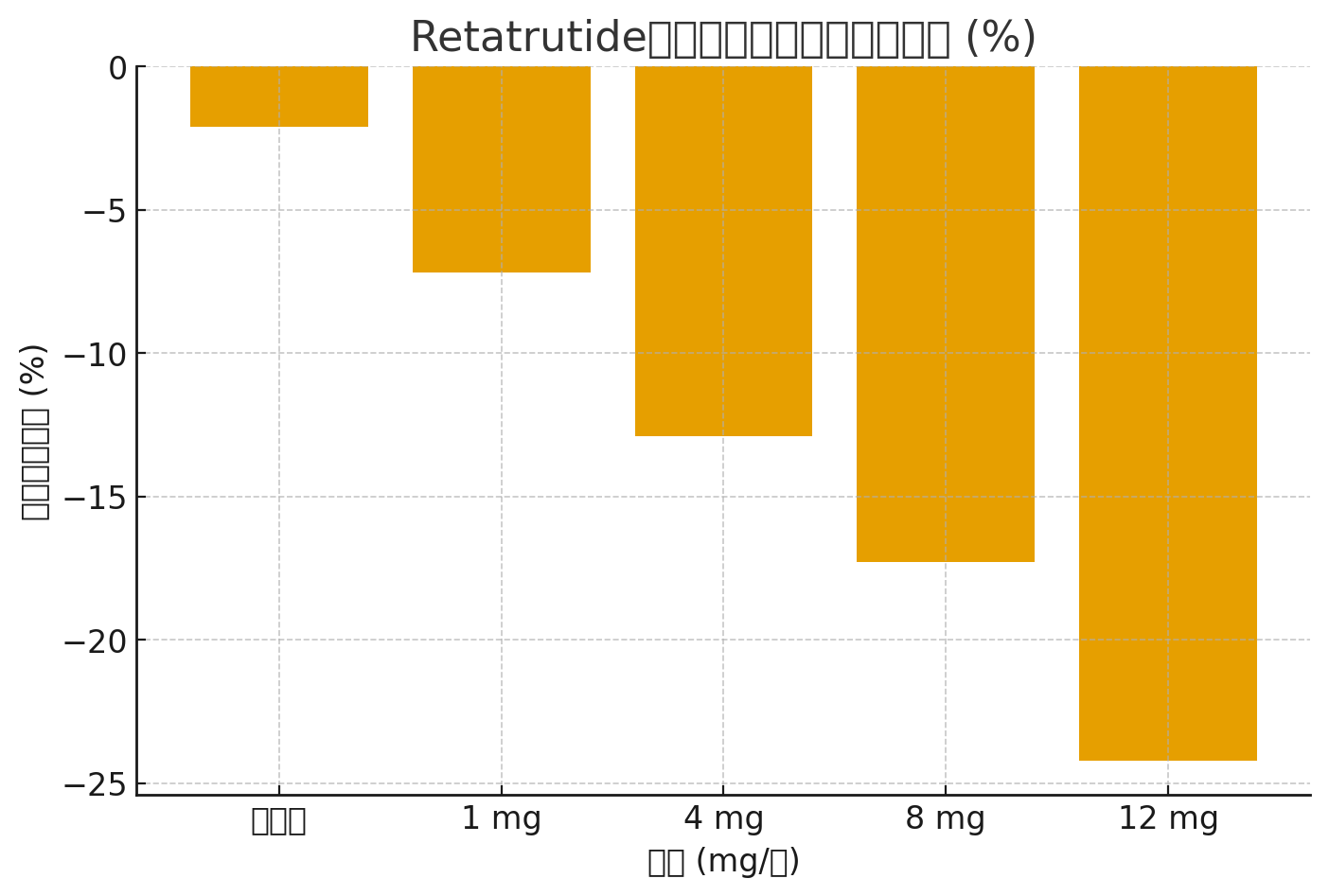
Datenvisualisierung (Vergleich der Gewichtsreduktion)
Das folgende Balkendiagramm veranschaulicht diedurchschnittliche Gewichtsreduktionüber verschiedene Retatrutid-Dosierungen im Vergleich zu Placebo:
Veröffentlichungsdatum: 16. September 2025